再生胰島臨床突破:
1型糖尿病治療迎來新路徑
 222
222
 訂閱已訂閱已收藏
訂閱已訂閱已收藏 收藏
收藏點擊播報本文,約

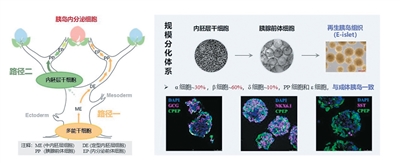 |
基於內胚層干細胞的胰島體外再造技術示意。 |
近日,中國科學院分子細胞科學卓越創新中心(生物化學與細胞生物學研究所)程新研究組聯合海軍軍醫大學第二附屬醫院殷浩團隊在線發表最新研究成果,在國際上首次分別利用自體與異體干細胞來源的再生胰島(E-islet)微創移植,實現了1型糖尿病患者的胰島功能重建與血糖自主調控。相關論文發表於國際學術期刊《柳葉刀·糖尿病與內分泌學》。
“零件”再造,開辟新技術路徑
糖尿病是嚴重威脅我國居民健康的慢性病,其中1型糖尿病多發病於兒童及青少年。
由於自身免疫紊亂、機體免疫系統異常攻擊並破壞胰島β細胞,導致胰島功能衰竭、胰島素分泌嚴重不足、血糖難以控制,長期以來被視作無法逆轉的慢性疾病。患者必須終身依賴胰島素注射與頻繁血糖監測,不僅承受長期治療的身心壓力,還可能引發腎臟衰竭、失明、心腦血管損傷、低血糖昏迷甚至死亡等嚴重並發症,極大威脅生命健康,也給無數家庭帶來沉重負擔。傳統的胰島移植雖有效,但受限於供體嚴重匱乏,無法惠及廣大患者。如何實現胰島組織的規模化再生,成為全球醫學界亟待攻克的難題。
如果把人體看作一台精密機器,那麼胰島功能的損傷,就像關鍵“零件”壞了。
“體外胰島再生,相當於給患者‘更換零件’。”程新這樣形容。過去,這個“零件”通常從“多能干細胞”開始制造。它就像一棵樹的“樹根”,理論上可以長成身體裡的任何細胞,潛力很大。但問題也在於此,從“樹根”長到最終需要的“胰島”,路徑太長、分支太多,不僅步驟復雜、周期漫長,在體外也很難精准控制方向。最終得到的細胞,往往純度不夠,還可能混入未完全分化,甚至在體內繼續增殖的細胞,帶來潛在風險。
研究團隊選擇了一條不同的路徑。“我們沒有再從‘樹根’走,而是直接從更接近目標的‘樹干’出發。”程新說,他們建立了一套基於內胚層干細胞的定向分化體系。
這個“起點”的改變,帶來了幾方面關鍵提升。首先,方向更明確。從一開始就限定在胰腺、肝臟等內胚層來源的細胞范圍內,相當於提前設好了“導航”,不會偏離到其他細胞類型。其次,流程更簡化。分化步驟從原來的十步減少到兩步,培養周期也從5—6周縮短到約2周,效率大幅提高。更重要的是,這類細胞在體內不具備增殖能力,從源頭上降低了成瘤風險,安全性顯著提升。
基於這一技術,研究團隊成功構建出可用於臨床的“再生胰島”(E-islet)。
在治療過程中,醫生通過肝門靜脈,將這些“再生胰島”輸注到患者體內。它們可以像正常胰島一樣工作,感知血糖變化並分泌胰島素,從而重新接管血糖調控功能。
臨床攻堅,三例患者見証功能重建
技術是否真正有效,關鍵在臨床驗証。
研究團隊在三例患者中,分別採用自體或異體內胚層干細胞來源的再生胰島開展臨床研究,並在不同免疫抑制策略下評估療效與安全性,臨床數據令人振奮。
三例不同年齡、不同病程的患者在接受自體或異體再生胰島移植后,均表現出胰島功能恢復與血糖控制改善的積極趨勢,同時進一步揭示了免疫抑制策略對療效維持的關鍵影響。
臨床病例涵蓋了世界首例自體與中國首例異體再生胰島移植治療1型糖尿病,以及世界首例再生胰島移植治療青少年1型的情況,其中最長一例已實現臨床治愈超過26個月。
研究團隊首次在國際上証明了,無論是自體還是異體來源的再生胰島移植,均可在1型糖尿病患者中實現胰島功能重建、血糖自主調控與外源胰島素脫離,從而長期改善患者的血糖水平、有效避免並發症的發生與進展。研究提示,該療法目前仍需聯合使用長期免疫抑制治療,用於克服1型糖尿病自身免疫復發等問題。
據了解,基於該自主知識產權開發的“異體人再生胰島注射液(E-islet 01)”已於2025年4月和2026年1月先后獲得中國和美國的新藥臨床試驗(IND)批件,是全球唯一同時獲批中、美兩國IND的再生胰島藥物。目前,臨床試驗正在嚴謹有序地開展,進展順利。
未來,研究團隊將通過基因編輯等手段進一步改造再生胰島,使其不再被免疫系統識別,從而規避免疫抑制劑的使用,最終達到完全治愈糖尿病的目標。
分享讓更多人看到 
- 評論
- 關注






























 第一時間為您推送權威資訊
第一時間為您推送權威資訊
 報道全球 傳播中國
報道全球 傳播中國
 關注人民網,傳播正能量
關注人民網,傳播正能量